双特异性抗体——现状与前景
双特异性抗体 (BsAb) 是具有两个结合位点的抗体,针对两种不同的抗原或同一抗原上的两个不同表位。双特异性抗体在临床上优于单克隆抗体(MoAb),在肿瘤免疫治疗以及甲型血友病、糖尿病、阿尔茨海默病和眼科疾病等其他疾病的治疗中具有广泛的应用。目前,全球已有9种双特异性抗体获批,超过180种双特异性抗体处于临床前开发阶段,超过50种双特异性抗体已进入临床试验。
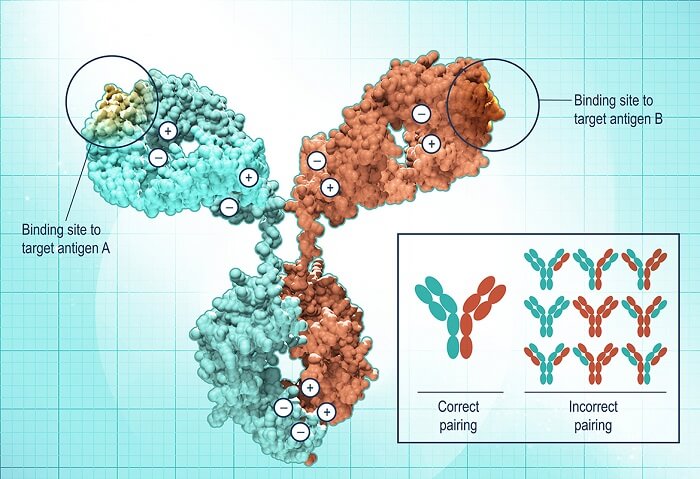
双特异性抗体如何发挥作用?
由于双特异性抗体具有两个针对不同抗原的结合位点或同时识别抗原的两个不同表位,因此它们的功能途径非常灵活。双特异性抗体有四种主要作用机制。
-
▶ 招募并激活免疫细胞,发挥杀伤作用
-
▶ 阻断双重信号通路
-
▶ 阻断免疫检查点
-
▶ 迫使蛋白质复合物缔合
免疫细胞的招募和激活
双特异性抗体的一个重要作用机制是激活免疫细胞。双特异性抗体有两个抗原结合臂,其中一个与目标抗原结合,另一个与效应细胞(常用 T 细胞和 NK 细胞)上的标记抗原结合,从而激活效应细胞并使其能够靶向和杀死肿瘤细胞。 CD3目前是双特异性抗体开发的流行免疫细胞表面靶标,具有更强的激活和招募T细胞的能力。
这种双特异性抗体的设计重点是选择合理的抗体亲和力范围,以尽可能抑制Fc介导的效应功能,同时对肿瘤靶点具有更强的特异性。已上市的blinatumomab(靶向CD3×CD19)去除了Fc结构并降低了T细胞过度激活的风险。两种抗体均使用不具有完整 IgG 结构的单链抗体片段,从而降低了 CD3 亲和力。还选择了肿瘤特异性较高的CD19靶点,安全性相对较好。
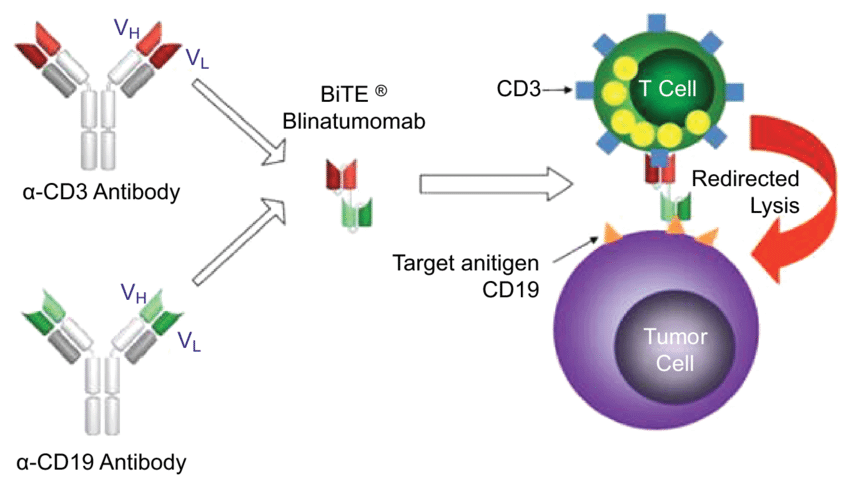
blinatumomab 的作用机制
阻断双信号通路
肿瘤细胞的生长可以通过受体酪氨酸激酶(RTK)(包括 Her 家族成员或胰岛素样生长因子(IGF))来模拟或调节。因此,RTK 是肿瘤治疗的重要靶点。针对RTK的单靶点单克隆抗体已广泛应用于肿瘤治疗。然而,肿瘤细胞可以通过切换信号通路或通过HER家族成员本身或不同成员之间的同源或异源二聚化激活细胞内信号来经历免疫逃逸。因此,利用双特异性抗体药物同时干扰/阻断两条(或更多)RTK信号通路或其配体可以减少肿瘤细胞逃逸,提高治疗效果。
阻断免疫检查点
随着免疫治疗的发展不断进步,针对PD-1、PD-L1、CTLA-4等免疫检查点的单克隆药物已成为肿瘤治疗的重要工具,但免疫检查点单克隆药物的临床疗效仍然有限,且疗效不佳。患者患病率仍然较低。多项临床试验显示,免疫检查点单克隆抗体的联合疗法比单一疗法具有更强的治疗效果。因此,基于联合药物产生的协同效应,针对2种免疫细胞表面抗原的双特异性抗体药物已成为研究热点。
迫使蛋白质复合物缔合
双特异性抗体的两个抗原臂可以结合不同的抗原。可以制造双特异性抗体,结合两个特定的蛋白质分子,形成功能复合物,可以代替缺失的功能蛋白质发挥作用。
例如,Emicizumab (Hemlibra®) 是一种重组、人源化、双特异性单克隆抗体,通过桥接 FIXa 和 FX 来恢复缺失的活化因子 VIII (FVIII) 的功能,以促进血友病 A 患者的有效止血。
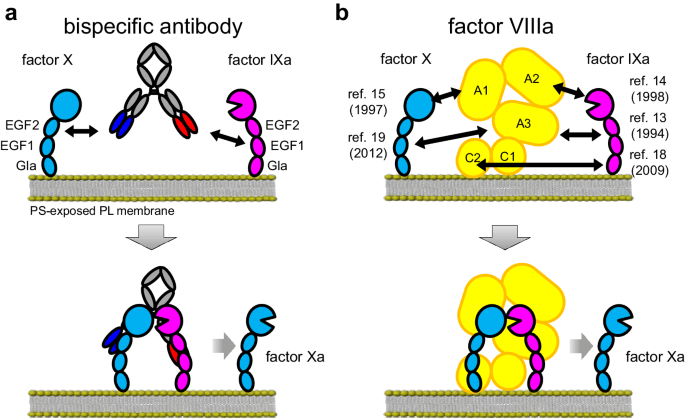
Emicizumab 的作用机制
双特异性抗体的临床优势
与传统抗体相比,BsAb 具有额外的特异性抗原结合位点,并已证明具有以下治疗优势。
-
1)介导免疫细胞对癌细胞发挥杀伤作用。
-
2)双重靶向免疫检查点,发挥重叠的功能,有效预防耐药性。
-
3) 增强特异性、靶向性并降低脱靶毒性。双特异性抗体的两个抗原结合臂可以结合癌细胞表面的两种抗原,有效增强抗体对癌细胞的结合特异性和靶向性,减少脱靶副作用。
-
4)有效降低治疗费用。例如,与传统抗体相比,BiTE在组织穿透率、肿瘤细胞杀伤效率、脱靶率和临床适应症等方面都具有较强的竞争优势,临床优势显着。尤其是在剂量方面,由于BiTE的治疗效果可以达到常规抗体的100-1000倍,因此剂量可以低至原始剂量的1/2000,从而显着降低药物治疗的成本。与联合疗法相比,双特异性抗体的成本也远低于两种单一药物组合的成本。
全球批准的双特异性抗体
目前,全球批准的双特异性抗体有12种,其中 FDA批准的双特异性抗体有7种,包括blinatumomab、emicizumab、amivantamab、tebentafusp-tebn、faricimab-svoa、mosunetuzumab和epcoritamab(表1)。
| 双特异性抗体药物批准 | |||||
| 药品名称 | 商品名称 | 公司 | 目标 | 批准日期(国家/地区) | 适应症 |
| 卡妥索单抗 | 移除 | 特瑞恩制药公司 | CD20/EpCAM | 2009年(2017年撤回) | 恶性腹水 |
| 博纳吐单抗 | 布林西托 | 安进 | CD3/CD19 | 2014 年 12 月(美国) | 复发性或难治性前体B细胞急性淋巴细胞白血病(ALL) |
| 艾美珠单抗 | 家庭天秤座 | 罗氏公司 | 固定/外汇 | 2017 年 11 月(美国) | A 型血友病引起的出血 |
| 阿米万他单抗-vmjw | 雷布雷万特 | 詹森 | EGFR/cMet | 2021 年 5 月(美国) | 非小细胞肺癌 |
| 特本特福斯普特宾 | 金特拉克 | 免疫核心 | GP100/CD3 | 2022 年 1 月(美国) | 不可切除或转移性葡萄膜黑色素瘤 |
| 法瑞西单抗 | 瓦比斯莫 | 基因泰克公司 | Ang-2/VEGF-A | 2022 年 1 月(美国) | 湿式 AMD 和 DME |
| 卡多尼利单抗 | 开坦尼® | 康方科技有限公司 | PD-1/CTLA-4 | 2022 年 6 月(中国) | 宫颈癌 |
| 莫苏奈妥珠单抗 | 伦苏米奥 | 罗氏公司 | CD20/CD3 | 2022 年 6 月(美国) | 复发性或难治性 (R/R) 滤泡性淋巴瘤 (FL) |
| 替克他单抗 | 特茨瓦伊利 | 詹森 | BCMA/CD3 | 2022 年 8 月(欧盟) | 复发难治性多发性骨髓瘤 |
| 奥佐拉珠单抗 | 纳米佐尔 | 大正制药 | 肿瘤坏死因子α/肿瘤坏死因子α | 2022 年 9 月(日本) | 炎症性疾病 |
| 格洛菲他单抗 | 哥伦维 | 罗氏加拿大 | CD3/CD20 | 2023 年 3 月(加拿大) | 弥漫大B细胞淋巴瘤 |
| 艾普利他单抗 | 埃普金利 | 美国Genmab | CD3/CD20 | 2023 年 5 月(美国) | 弥漫大B细胞淋巴瘤 |
表 1. FDA 和 EMA 批准的双特异性抗体
-
▶ 2014年,安进公司的blinatumomab(Blincyto)被FDA批准用于治疗复发或难治性前体B细胞急性淋巴细胞白血病(ALL),具有CD3/CD19双靶点。 2015年晚些时候,它获得了EMA的批准。
-
▶ 随后在 2017 年,罗氏的 emicizumab (Hemlibra) 被批准用于治疗 A 型血友病引起的出血,通过形成蛋白质复合物作用于 FIXa/FX 因子。 2018年晚些时候,它获得了EMA的批准。
-
▶ 2021 年 5 月 21 日,FDA 批准阿米万他单抗-vmjw (Rybrevant)用于治疗成年非小细胞肺癌患者,靶向表皮生长因子受体 (EGFR) 和间充质-上皮过渡因子 (MET) 通路。而且,Rybrevant于 2021 年 12 月 9 日获得了在整个欧盟有效的有条件营销。
-
▶ 2022 年 1 月 25 日,FDA 批准 tebentafusp-tebn (Kimmtrak,Immunocore Limited),一种双特异性 gp100 肽-HLA 导向的 CD3 T 细胞接合剂,用于治疗不可切除或转移性葡萄膜的 HLA-A*02:01 阳性成年患者黑色素瘤。
-
▶ 2022 年 1 月 28 日,血管内皮生长因子 (VEGF) 抑制剂和血管生成素-2 (Ang-2) 抑制剂 Vabysmo (faricimab-svoa) 被批准用于治疗湿性或新生血管性年龄相关性黄斑变性 (AMD ))和糖尿病性黄斑水肿(DME)。
-
▶ PD-1/CTLA-4双特异性抗体开坦尼®(卡多利单抗注射液,AK104)已获得中国国家药品监督管理局(NMPA)上市批准,用于治疗复发或转移性宫颈癌(R/M) CC)在铂类化疗期间或之后出现进展的患者。
-
▶ 2022年6月8日,罗氏宣布欧盟委员会授予CD20xCD3 T细胞结合双特异性抗体Lunsumio(mosunetuzumab)有条件营销,用于治疗至少接受过两次治疗的复发或难治性(R)疾病患者先前的全身治疗。 /R) 成人滤泡性淋巴瘤 (FL) 患者。
-
▶ 2022 年 8 月 24 日,强生旗下杨森制药公司宣布,欧盟委员会 (EC) 已授予 TECVAYLI®(teclistamab)有条件营销(CMA),作为单药治疗成人复发难治性多发性骨髓 瘤 患者骨髓瘤(RRMM)。 2022年10月25日,FDA加速批准Tecvayli。
-
▶ Ozoralizumab(商品名 Nanozora)是一种人源化单克隆抗体,设计用于治疗炎症性疾病。 2022 年,ozoralizumab 在日本获批用于治疗类风湿关节炎。
-
▶ Hoffmann-La Roche Limited(罗氏加拿大公司)宣布,加拿大卫生部于2023年3月24日COLUMVI®(注射用格洛菲他单抗) 用于治疗复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)成年患者。
-
2023年5月19日, FDA加速批准epcoritamab-bysp(Epkinly,Genmab US,Inc.)用于治疗复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)。
-
▶ 顺便说一下,Catumaxomab 于 2009 年 4 月 20 日在欧洲获得批准。但由于商业原因,Catumaxomab 在 2013 年自愿从美国市场撤回,并于 2017 年从欧盟市场撤回。
后期管道
双特异性抗体的后期临床开发管道大部分是双特异性 T 细胞桥接剂,其作用是重定向和激活表达 CD3 的细胞毒性 T 细胞,以靶向并杀死表达特定抗原的肿瘤细胞。
在血液癌症中,主要靶标是 CD20 和 B 细胞成熟抗原 (BCMA)。在实体瘤中,主要靶点是CTLA4、PD-1/PD-L1、LAG3、EGFR和HER2/HER3。部分已进入3期临床阶段的双特异性抗体见下表。
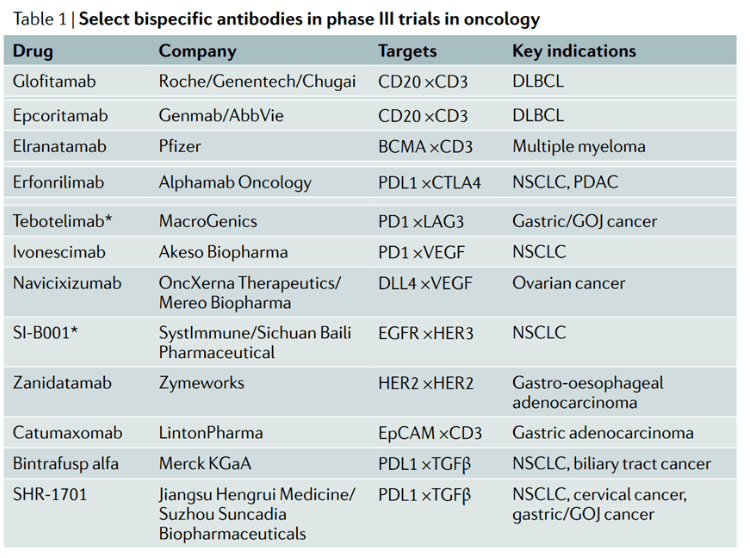
精选肿瘤双特异性抗体处于3期临床开发(数据来源:参考文献[1])
早期管道
在早期临床开发中,多种双特异性抗体针对现有或创新靶点。在血液肿瘤的治疗方面,正在或计划注册临床试验的双特异性抗体包括Regeneron和AbbVie的BCMAxCD3双特异性抗体、Janssen的GPRC5DxCD3双特异性抗体talquetamab、MacroGenics的用于治疗急性髓系白血病的CD123xCD3双特异性抗体flotetuzumab和Affimed的用于治疗急性髓系白血病的CD30xCD16A双特异性抗体AFM13外周 T 细胞淋巴瘤等。
在实体瘤方面,多个潜在的注册 1/2 期临床试验正在进行中。请参阅下表,了解一些正在开发的疗法的信息。
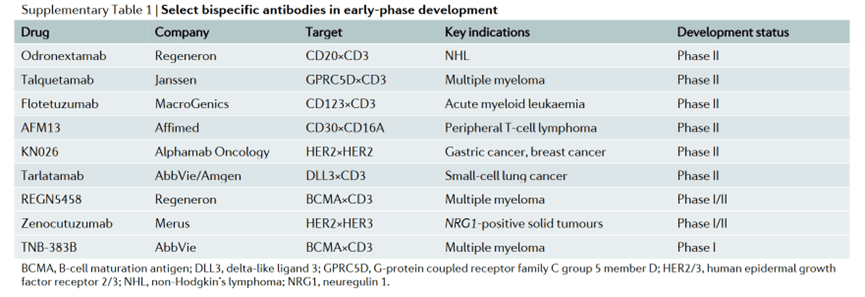
早期临床开发中的精选双特异性抗体疗法(数据来源:参考文献[1])
未来发展
全球肿瘤学双特异性抗体市场预计将迅速扩张,到 2027 年销售额可能达到 37 亿美元。在血液癌症中,靶向 CD20xCD3 的双特异性抗体疗法预计将带来 CAR-T 细胞疗法和既定靶向疗法之外的重要新治疗选择适用于 B 细胞非霍奇金淋巴瘤和弥漫性大 B 细胞淋巴瘤患者。在实体瘤中,针对不同 HER2 表位的扎尼达单抗可能使大量 HER2 阳性胃食管腺癌患者受益。
除了肿瘤的治疗之外,双特异性抗体疗法还是治疗炎症性疾病以及其他疾病类型的重要治疗方式。它们还具有多种其他作用模式,例如帮助大分子穿过血脑屏障并充当激活信号级联通路的辅助因子。我们期望这种创新的治疗方式未来将惠及更多患者。
Biopharma PEG作为PEG供应商,为您的药物研发提供高质量的PEG衍生物和原材料。这些化合物具有良好的水溶性、广泛的聚合物长度/重量以及所有流行官能团的广泛选择。
