如何选择染料
为了使用荧光标记物获得最佳结果,必须考虑几个因素。
首先,这是激发光源:为了减少样品自发荧光可能产生的干扰,激发波长优选在550 nm甚至600 nm以上。除了减少背景之外,红色光谱范围在处理活细胞时也具有优势,因为可以减少损伤。
其次,荧光标记应在激发波长下具有强吸收以及高荧光量子产率。消光系数和荧光量子产率的乘积通常称为染料的“亮度”。
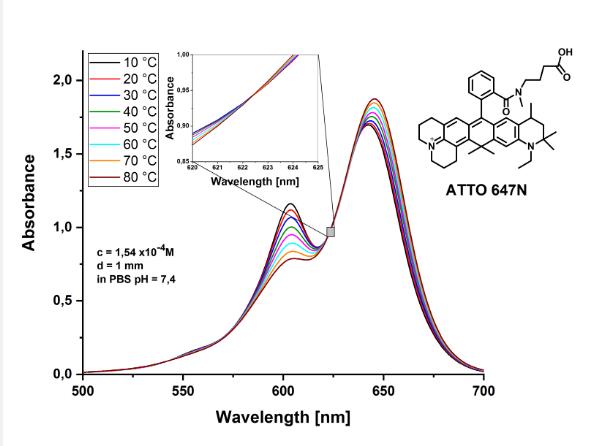
染料的荧光效率在光谱的蓝色和绿色区域最高。在某些情况下,量子产率几乎达到100%的理论极限。对于更长的波长,发射的量子产率急剧下降,尤其是在水溶液中。然而, ATTO-TEC已成功开发出即使在 650 nm 下也具有高量子产率的荧光标记。例如,ATTO 647N在水溶液中发出的荧光强度是旧花青染料 Cy5 ™的两倍。ATTO 647N和 Cy5 ™的相对荧光强度。PBS 水溶液1 cm 池中相应吸收最大值处的吸光度为 0.04。22 °C 时两个吸收光谱(相同吸收)交叉处的荧光激发。
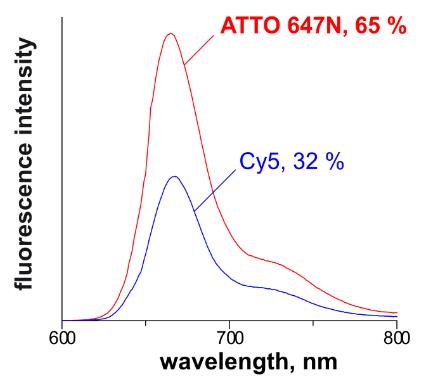
最后,标记物的发射光谱应与所用滤光片组的传输相匹配。反过来,必须选择滤光片组,使其阻挡样品散射的激发光并允许荧光尽可能有效地通过。
当使用波长为 635 nm 的二极管激光器作为激发源以及在 650 nm 至 750 nm 之间具有高透射率的滤光片组时,例如ATTO 647N将是一个非常好的选择。从ATTO染料列表可以看出, ATTO647N635 nm处具有高消光系数,接近吸收曲线最大值的波长,以及优异的荧光量子产率(η fl = 65%)。
下表概述了一些常用的激励源和推荐的ATTO标签。
| 光源 | 发射线 | 适用染料 |
|---|---|---|
| 水银蒸气灯 | 365纳米 405纳米 436 纳米 546纳米 577纳米 |
ATTO 390 ATTO 425、ATTO 430LS ATTO 425、ATTO 430LS、ATTO 465 ATTO 550、ATTO 565 ATTO Rho12、ATTO Rho101、ATTO 590 ATTO Rho13、ATTO 594、ATTO 610、ATTO Rho14 |
| 氩离子激光器 | 488nm 514nm |
ATTO 488、ATTO 490LS ATTO 514、ATTO 520 ATTO 514、ATTO 490LS、ATTO 520 ATTO 532、ATTO 542 |
| Nd:YAG 激光器, 倍频 |
532纳米 | ATTO 532、ATTO Rho6G、ATTO 542 ATTO 550、ATTO 565、ATTO Rho11、ATTO Rho12 |
| 氦氖激光器 | 633纳米 | ATTO 643、ATTO 633、ATTO 647、 ATTO 647 N、ATTO 655 |
| 氪离子激光器 | 647nm 676nm |
ATTO 643 ATTO 647、ATTO 647 N、ATTO 655、 ATTO Oxa12、ATTO 665、ATTO 680 ATTO 680、ATTO 700、ATTO 725、ATTO 740 |
| 二极管激光器 | 635纳米 | ATTO 633、ATTO 643、ATTO 647、 ATTO 647 N、ATTO 655 |
荧光标记物的特性
然而,应该注意的是,除了已经讨论的光学考虑因素之外,选择标记时其他因素也很重要,例如染料的 pH 依赖性光学和化学特性、其溶解度、光和化学特性稳定性、发色团的大小或连接体的长度等,其涉及或满足各自应用的要求。这些特性与染料作为荧光标记物的适用性非常相关。
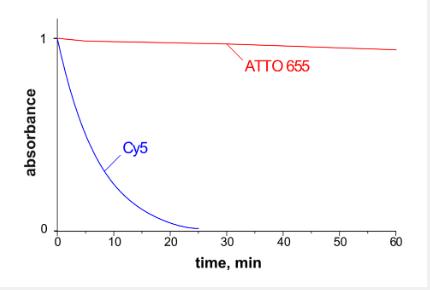
最重要的是,染料在照射过程中保持完整。许多常见的标记,例如荧光素衍生物 FITC,具有非常低的光稳定性。因此,当长时间观察过程时,使用高强度激光激发时成像的灵敏度和质量会受到限制。这对于显微镜和其他基于共焦原理的技术(例如单细胞的检测)来说是一个严重的缺点。与一些常用的旧染料相比,新型ATTO标签的设计即使在长时间暴露后也显着更加稳定。
ATTO 655与传统 Cy5的光稳定性比较TM在水里。使用 250 W 卤钨灯照射,聚焦到 1 cm 池中。消光与照射持续时间。
许多常见的荧光标记物即使在没有照射的情况下(即在黑暗中)也会分解,特别是当暴露于实验室大气中的低浓度臭氧时。在相同的臭氧暴露条件下,染料ATTO 647N和ATTO 655的稳定性比花青染料 Cy5 TM和 Alexa647 TM长 100 倍。这在微阵列应用中非常重要,因为染料分子位于表面,因此直接暴露在大气中。
紧凑而强大的激光二极管现在覆盖了光谱的整个可见光和近红外部分。它们已作为非常有效的激发源进入许多应用/设备,并越来越多地取代传统光源。
如果没有最大吸收与现有激发源的波长完*对应的标记,则应选择波长稍长的染料。吸收会稍微降低,但激发波长和荧光光谱之间的较大差异(与激发波长无关)具有在检测过程中更好地分离散射激发光的优点。