细胞外囊泡的临床蛋白质组学分析
-关于血液循环细胞外囊泡的多样品自动纯化技术的开发-
![]()
医药基础·健康·营养研究所 蛋白质组研究项目 村冈贤、足立淳
◆前言
近年来,在癌症、神经疾病、心血管疾病、传染病等各类医学研究领域中,都在不断展开细胞外囊泡的研究。细胞外囊泡中含有蛋白、核酸和脂质等,这些组成成分因细胞或疾病而异,并且因其具有多种功能,会对疾病的病理变化产生很大的影响。因此,从血液等样品中提取的细胞外囊泡中用于疾病早期发现、监测、药效分析等的生物标志物,备受人们期待。
在本文中,作者会介绍至今为止进行过的神经退行性疾病相关的细胞外囊泡的功能分析和对生物标志物的探索,以及面向大规模蛋白质组学分析的用于血液来源细胞外囊泡的多样品自动纯化技术。
◆细胞外囊泡
细胞外囊泡是由各种组织和细胞分泌的被脂质双层膜所包围的膜囊泡的总称。由于分泌路径、生物合成和尺寸的不同,细胞外囊泡分为由多囊泡和细胞膜融合分泌到细胞外的外泌体(40-200 nm);直接从细胞膜出芽并分泌到细胞外的微泡(200-1000 nm);从发生细胞凋亡的细胞中分泌的凋亡小体(1000-5000 nm)这三类。我们可以从血液、尿液、唾液和脑脊液等体液中观察-到细胞外囊泡,其中包含各种蛋白、核酸和脂质等,对于细胞间的信息传递尤为重要1)。
近年来,众多研究表明细胞外囊泡与恶性肿瘤、炎症性疾病和神经疾病等疾病相关,因此在探索用于疾病诊断,预后预测的生物标志物和面向治疗的应用研究中,细胞外囊泡备受期待2)。此外,由于使用血液中细胞外囊泡的诊断属于微创诊断,可减轻患者在长期观察中的负担,同时捕捉疾病的变化,所以急需开发此类诊断方法。
◆神经退行性疾病相关的细胞外囊泡
随着年龄增长,神经退行性疾病的患病风险也会升高,所以对于老龄化日渐加剧的日本来说已是不容忽视的一类疾病。关于细胞外囊泡在阿尔茨海默病、肌萎缩侧索硬化症和帕金森病等神经退行性疾病中作用的研究,在近10年已取得显著进展。
2006年Rajendran等人报告阿尔茨海默病病因之一的β淀粉样蛋白存在于细胞外囊泡的内外,并且细胞外囊泡的特异性蛋白ALIX存在于阿尔茨海默病患者大脑内的淀粉样斑块3)。2012年Saman等人发现在过度表达致病因子之一的Tau蛋白的细胞中,分泌的细胞外囊泡内存在Tau蛋白4)。
笔者已确认阿尔茨海默病患者脑组织来源的细胞外囊泡中存在的Tau蛋白中对聚集体形成非常重要的Serine396发生了磷酸化(pS396 tau)。其与对照组比较有显著地上升(图1a,b)5)。另外,还确认到其Tau蛋白是以寡聚体的状态存在于细胞外囊泡内,作为小鼠、细胞实验中用于传播,聚集Tau的种子,与细胞外囊泡共同具有着重要的功能6)。
此外,通过蛋白质组学分析了阿尔茨海默病的脑组织来源(蔗糖密度梯度离心法),脑脊液来源(MagCapture™ Exosome Isolation Kit PS;FUJIFILM Wako,293-77601)的细胞外囊泡,比较ANXA5、PTGFRN和对照组发现这些蛋白的表达有所上升(图1c,d,e)5,7)。
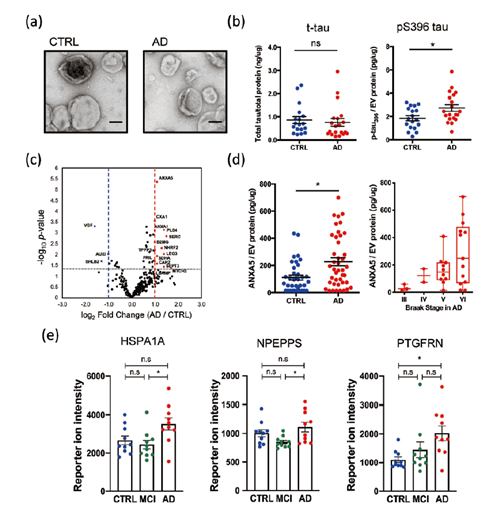
图1. 神经退行性疾病中细胞外囊泡的功能和生物标记开发
(a)透射电子显微镜下的细胞外囊泡 (b)存在于细胞外囊泡内外的Tau和磷酸化Tau (c)基于蛋白质组学分析的蛋白质表达量比较 (d)阿尔茨海默病患者脑组织来源细胞外囊泡的ANXA5的表达上升 (e)脑脊液来源细胞外囊泡的生物标记候选蛋白
CTRL:健康 MCI:轻度认知障碍 AD:阿尔茨海默病性痴呆 *:p < 0.05
虽然使用脑脊液监测疾病是优选,但提取脑脊液对患者来说负担沉重,所以希望能有微创的血液检查。因此笔者等人考虑使用多个检测样品的血液样品细胞外囊泡分析和评估候选蛋白,为了同时处理多个样品,并且消除人工操作的误差,我们开发了可自动纯化体液来源细胞外囊泡的技术。
◆血清和血浆来源细胞外囊泡的自动纯化技术开发
体液中含有大量的细胞外囊泡,考虑到其还包含了来源细胞的变化,因此使用大规模的临床检测样品进行细胞外囊泡蛋白的全面蛋白质组学分析正在盛行。至今已报告许多从血液中浓缩细胞外囊泡的方法,例如组合式离心法、平衡密度梯度离心法、尺寸排阻色谱法、利用亲和性的纯化法等8)。
由于不同方法分分离的细胞外囊泡也各异,而且含有杂质的比例也不同,所以可高纯度纯化细胞外囊泡的方法,以及标准化纯化方法非常必要。其中,基于与细胞外囊泡的磷脂酰丝氨酸具有高亲和性的Tim4蛋白的纯化法,与其他方法相比,可大幅度地抑制减少杂质并进行高纯度浓缩9,10)。
高纯度纯化和浓缩细胞外囊泡可以降低蛋白的动态范围,能够在蛋白质组学分析中定性和定量微量蛋白。此外,为了实现大规模临床样品的蛋白质组学分析,开发重复性高的纯化系统尤为重要。
笔者等人通过使用96孔正压萃取装置对 96 份血清和血浆样品进行过滤前处理,并在 KingFisher Flex系统上使用了 MagCapture™ Exosome Isolation Kit PS,成功开发了一次性纯化96份样品的自动纯化技术(图2)。
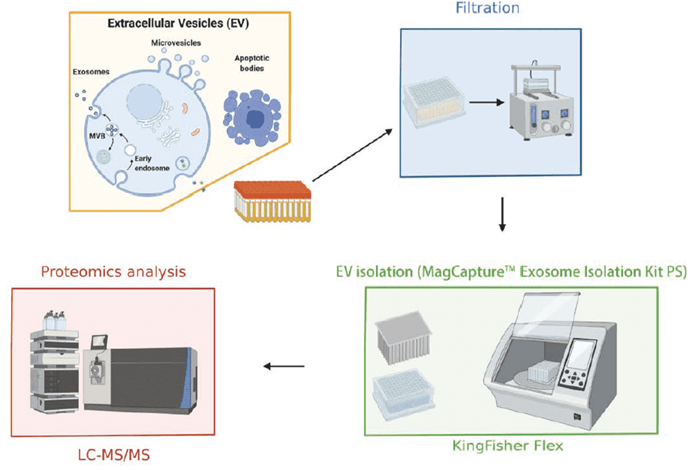
图2. 使用MagCapture™ Exosome Isolation Kit PS开发细胞外囊泡的自动纯化技术的开发
◆血清和血液细胞外囊泡的蛋白质组学分析
笔者等人在通过对自动纯化技术纯化的细胞外囊泡进行了全面蛋白质组学分析,发现与手动纯化相比,自动纯化技术可以降低样品间的差异,在提高细胞外囊泡标志物的离子强度的同时,还能大幅度降低血液蛋白中的载脂蛋白B的离子强度(图3a)。
使用临床样品的分析中,成功定性了细胞外囊泡标志物在内的4079种蛋白,发现血清和血浆来源的细胞外囊泡中有部分蛋白的定量值差异较大(图3b)11)。需要根据研究目的选择血清或血浆中的评估用蛋白。
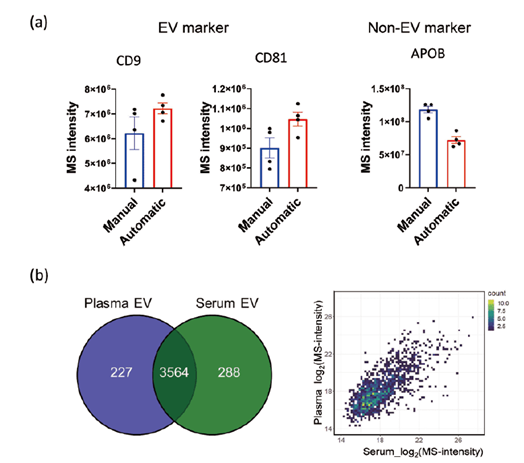
图3. 自动纯化的血清和血浆来源细胞外囊泡的蛋白质组学分析
(a)手动和自动纯化的细胞外囊泡标志物的比较 (b)血清和血浆来源细胞外囊泡的蛋白质组学分析的结果
目前,研究人员使用自动纯化技术进行大规模临床样品的蛋白质组学分析,成功定性了脑组织来源细胞外囊泡的候选特异性标志物蛋白11)。
◆结语
液体活检可以从含有血液或尿液的体液中检测或监测癌症、退行性疾病和传染病等,是一种备受期待的检测、监测方法,因此将细胞外囊泡应用于液体活检也备受瞩目,期待今后可以得到进一步的研究和开发。血液细胞外囊泡的蛋白质组学分析,不仅在标志物的探索,在阐明病理的机制中也能发挥作用,对于大规模临床样品分析有着重要作用。
本次我们开发的自动纯化技术可同时处理多个样品,重复性优异,还可以抑制血液蛋白的污染。此外,我们还实现了蛋白质组学分析前处理的自动化(论文投稿中),有望为疾病生物标志物探索以及诊断试剂盒的开发提供新的技术。
◆谢辞
神经退行性疾病的细胞外囊泡的研究是在波士顿大学(现Mayo clinic)池津庸哉老师的带领下进行的,细胞外囊泡的自动化纯化是在富士胶片和光纯药株式会社的协助下在医药基础研究所进行的。在此,表示衷心地感谢。
◆参考文献
1. Kowal, J. et al. : Proc. Natl. Acad. Sci. U.S.A., 113, E968 (2016).
2. Shiromizu, T. et al. : Sci. Rep., 7, 12782 (2017).
3. Rajendran, L. et al. : Proc. Natl. Acad. Sci. U.S.A., 103, 11172 (2006).
4. Saman, S. et al. : J. Biol. Chem., 287, 3842 (2012).
5. Muraoka, S. et al. : Alzheimers Dement., 16, 896 (2020).
6. Ruan, Z. et al. : Brain, 21, 72 (2020).
7. Muraoka, S. et al. : Cells, 9, 1959 (2020).
8. Li, P. et al. : Theranostics, 7, 789 (2017).
9. Nakai, W. et al. : Sci. Rep., 6, 33935 (2016).
10. Muraoka, S. et al. : Methods, 177, 35 (2020).
11. Muraoka, S. et al. : iScieuce, (2022) in press, DOI 10.1016/j.isci.2022.104012
◆相关产品
|
产品编号 |
产品名称 |
包装 |
|
293-77601 |
MagCapture™ Exosome Isolation Kit PS |
10 tests |
|
299-77603 |
2 tests |
|
|
290-84103 |
MagCapture™ Exosome Isolation Kit PS Ver.2 |
10 tests |
|
294-84101 |
2 tests |
※ 本页面产品仅供研究用,研究以外不可使用。